|
�������
����һ����״�������������Ĥ��֯ϸ�������������ˮƽ�ıȽ�
������״������������Ĥ��֯������������������Һ�о��ܲTNF-����PDGF�Ļ��ԣ�����״����������Ը����������Ĥ��(P��0.01)����1����
��1��30����״�������״������������Ĥ
������֯�е�ϸ�����ӷ��ڱ���
| ��� |
���� |
TNF-��
����(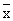 ��s����10-12g/mg����) ��s����10-12g/mg����) |
PDGF
����(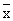 ��s��U/mg����) ��s��U/mg����) |
| ��״���� |
30 |
43.8��22.1 |
71.3��12.4 |
| �������Ĥ |
30 |
��9.4��3.6 |
��8.9��4.7 |
| tֵ |
�� |
2.827 |
3.011 |
| Pֵ |
�� |
��0.01 |
��0.01 |
����������ͬʱ�ڵ���״������֯ϸ�����ӷ���ˮƽ�ıȽϣ���2��
��2��30����״����߲�ͬʱ�ڵ���״����
������֯��ϸ�����ӷ���ˮƽ�ıȽ�
| ��� |
���� |
TNF-��
����(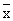 ��s����10-12g/mg����) ��s����10-12g/mg����) |
PDGF
����(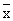 ��s��U/mg����) ��s��U/mg����) |
| ������ |
19 |
56.6��23.8 |
84.2��9.7 |
| ��ֹ�� |
11 |
29.2��14.3 |
35.1��8.5 |
| tֵ |
�� |
2.374 |
2.712 |
| Pֵ |
�� |
��0.05 |
��0.05 |
������������״������֯�е�TNF-����PDGF��������������Ը��ھ�ֹ����״������֯(P��0.05)�����������������кͿ������״������֯�������TNF-����PDGF��Ӱ��
������������״���⣬��������Һ�飬��������������Һ��TNF-����PDGF�ĺ������������2���ӿ�TNF-�������飬��������������Һ�е�PDGF����Ϊ(47.6��7.8)U/ml���ף����Ե��ڵ�������Һ���PDGF���ԣ�t��2.265��P��0.05�����ӿ�PDGF�����飬��������������Һ�е�TNF-������Ϊ(30.9��13.3)��10-12g/mg���ף����Ե��ڵ�������Һ���TNF-��������t��2.196,P��0.05����
��������
����һ����״�����γɵ�ԭ��
������״������γ��Ƕ������ز���ĸ��Ӳ������̡���ԭ��Ϊ����άϸ���� ��Ƥϸ�����ܰ�ϸ����ѪС�弰����ϸ����������õ��´��������ij���άϸ����Ѫ�ܵ��������˱���4�������⣬�ò������������䡢��ɳ���۳��� �����ݼ�����Ⱦ���йأ�����Щ���ؾ��ɵ������Ĥ�ĵ��ױ��Լ�ϸ�����ӵķ����쳣��5������ˣ�������ѧ����Ϊ��������������״����ķ���������Ҫ���á�
��������ϸ����������״���ⷢ�������е�����
����TNF-����PDGF��һ����Դ���ܰ�ϸ�������˾���ϸ����Ѫ����Ƥϸ����ϸ�����ӣ����Dz���һ�����Խ��ʣ����һ����Դٽ���άĸϸ������ֳ��6�������о��У���״������֯��������Һ�е�TNF-��������PDGF���Ծ����Ը����������Ĥ�飬�ҽ������뾲ֹ���������������ԣ�P��0.05��������TNF-����PDGF �ı����쳣��������״����ķ�����չ�йء������ױ�������״������֯���д���������Ѫ�ܡ���άĸϸ������ά���������ɼ��������ܰ͡���ϸ������ͷʴ�ϸ����Ӧ��7��8�����ⲻ����������״���ⷢ���������������صĴ��ڣ�������Щ���ؿɵ���TNF-����PDGF�ķ��ڱ���������9������ʹ��άĸϸ������ԭ��ά������������ϸ���Ľ��ٽ���״����ķ�չ��
��������TNF-����PDGF�����������
����McAvoy����10��������TNF-����PDGFͬ��ϸ�����������к��ij�Ա�����о��У���TNF-���� ���PDGF�IJ�������PDGF�����TNF-���IJ��������и���������ã�˵��TNF-����PDGF��ϸ�����������о�����ĵ������á���ˣ���һ���о���ζ�ϸ�����ӵķ��ڽ�����Ч�ĵ��أ�����״�����Ԥ�������Ƽ���ֹ�临����������Ҫ�����塣
���������
����[1]��Hill JC, Maske R. Pathogenesis of pterygium. Eye,1989,3:218-226.
����[2]��Thoratoay SC. Interaction of immune and connective tissue cells the effect of lymphokines and monokines on fibroblast growth. J Leuko Biol,1990,47:312-316.
����[3]��Heldin CH, Westermark B, Wasteson A. Platelet-derived growth factor: isolation by a large-scale procedure and analysis of subunit composition.Biochem J, 1981,193:907-913.
����[4]��Kria L, Ohira A, Amemiya T. Immunohistochemical localization of basic fibroblast growth factor, platalet derived growth factor, transforming growth factor-�� and tumor necrosis factor-�� in the pterygium. Acta Histochem,1996,98:195-201.
����[5]��Coroneo MT. Pterygium as an early indictor of ultraviolet insolation:a hypothesis. Br J Ophthalmol,1993,77:734-739.
����[6]��Gospodaroicz D,Neufeld G,Schweigerer L. Fibroblast growth factor. Mol Cell Endocrinol,1986,46:187-204.
����[7]��Xu GX, Tong Y, Lin FS, et al. Pathological study of pterygium. Invest Ophthalmol Vis Sci,1995,36:1027-1031.
����[8]�����֣��������IJ��������.��״��������߲���ѧ�о�. �л��ۿ���־,1993,29 :141-143.
����[9]��Kohase M, May LT, Tamm I, et al. A cytokine network in human diploid fibrolast interactions of ��-interferons, tumor necrosis factor, platelet-derived growth factor and interleukin-1.Mol Cell Biol,1997,7 :273-281.
����[10]��McAvoy JW,Chamberlain CG. Growth factors in the eye. Prog Growth Factor Res, 1990,2:29-43.
(�ո壺1998-06-22�����أ�1998-09-28) ��һҳ [1] [2] |
