|
����2���ᡡ��
����2.1����ˮ��ϸ������������Ĥ���鷿ˮ�ڵ�����ϸ����Ŀ�϶��������ȵ����ߣ�L-NAME���� (0 h)ʹ����������������ϸ��������(P��0.05), �� 6 h��������û����������(��1)��
����2.2����ˮ����Ũ�ȡ�����Ĥ���д����ĵ���������ǰ����L-NAME����(0 h)�������Խ����˵���Ũ�ȣ�������Ĥ����������������(P��0.05)����6 h������û����������(��1)��
����2.3����ˮ��������NO�����ĸı䡡�����������飬���нϵ�ˮƽ��NO������Ĥ��ʱ�������ߣ�����(0 h)������������NO�ĺ�����6 h������NO�����ı�������Ĥ����û�����Բ���(��1)��
����2.4����֯������顡����Ĥ�����ǰ���д���ϸ�������͵������۳ɿ飬��ĤѪ�����ų�Ѫ����Ĥ���ʲ�ͽ�״���д�������ϸ������L-NAME����(0 h)�����飬��Ĥ��Ѫˮ�ף�������������ά����������ϸ���ۼ�����Ĥ���ʼ���״�������ϸ���������Լ��ᣬL-NAME6 h������û�����Եĸ��ơ�
��1����ˮ��ϸ����Ŀ������Ũ�ȣ���ˮ�벣������NOŨ�ȼ���֯��֢�̶Ƚ��
����tab 1��The results of leukocyte number and protein concentration in aqueous humor, nitric oxide concentration
����in aqueous and vitreous humors and histopathologic examination(n=12,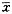 ��s) ��s)
| Group |
Leukocyte
����in AH (��109/L) |
Protein
����in AH (��B/g��L-1) |
NO in AH
����(cB/��mol��L-1) |
NO in VH
����(cB/��mol��L-1) |
The degree of
����inflammation |
| Control |
0.002��0.001 |
0.462��0.276 |
34.362�� 6.483 |
27.642�� 6.163 |
0 |
| Uveitis |
9.048��1.685* |
25.359��5.435* |
238.624��40.536* |
215.367��38.716* |
3.85��0.15* |
| Treatment (0 h) |
1.839��1.027���� |
5.417��1.541���� |
61.687�� 8.275���� |
55.683�� 7.475���� |
1.50��0.47���� |
| Treatment (6 h) |
9.672��1.966 |
19.593��4.847 |
216.362��25.138 |
186.392��23.162 |
3.63��0.36 |
����*P��0.05 vs control; ����P��0.01 vs uveitis; aH: Aqueous humors; VH: Vitreous humors
����3���֡���
��������Ĥ�ķ�����չ���ж�����֢���ʺ�ϸ�����Ӳ���Ĺ��̡������о�����NO��Ϊ��Ҫ���źŷ��Ӻ�ЧӦ���ӣ�������֢��Ӧ�����߷�Ӧ��(1) nO����Ϊ��ʹ���Ӽ���cGMP������Ѫ��ƽ�������ţ�Ѫ��ͨ�����ӣ���ϸ���͵�����Ѫ���������������3����(2) nO���յ���֬���Ǽ���ľ���ϸ�����ܰ�ϸ������ TNF���� IL����֢���ӣ��ٽ���֢��Ӧ��4����(3) nO�ɼ������ø��ʹǰ�����صĺϳ�������5����(4) nO������֢��Ӧ�в�����O2��������γɹ���������������( ONOO��)��������������һ��ǿ�����������ɷֽ�Ϊ���ֶ��Բ��һ����������ϸ��������лͨ·��Ĥ���ܵ��ƻ�������Ѫ-��ˮ���ϵĽṹ�����Ա��ƻ�����һ���������� sOD�����Ĺ�������ø��������Ҫ�Ŀ�������ϵ����������֯��������6�������о������ʾ����Ĥ��ˮ����������NOŨ���������ߣ�0 hʹ��L-NAME����NOŨ�ȵ�ͬʱ����ˮ�ڵ���Ũ�ȡ�����ϸ����Ŀ����֯��֢����̶ȵȸ�����ָ֢�����Լ��ᣬ˵��NO�ܴٽ�����Ĥ�ķ�չ��
����NO���� L-������Ϊ������һ��������ø (NOS)�Ĵ��ºϳɵģ� nOS��Ҫ��ΪcNOS��iNOS (inducibe NOS)��ǰ�ߴ��ϳ�������NO�����ߴ��ϳɴ�����NO��1����L-NAME��Ҫ���� cNOS�������� iNOSǿ100����7���� iNOS������LPSע���9 h�ﵽ�߷���8������ʵ������ʾ6 hʹ��L-NAMEû�����Խ���NO������û����ֹ����Ĥ�ķ�չ�����������iNOS���������ϲ��йء�0 hʹ��L-NAME����������Ĥ�ķ�չ����ʱ��iNOS���ϳɴ���NO�Ĺ��̻�û�п�ʼ����ʾ��cNOS���ϳɵ�����NO��������������Ĥ��ʼ�����̡���֮��NO������Ĥ���е����û��ƿ����Ʋ�Ϊ����cNOS���ϳɵ�����NOʹѪ�����ţ���ϸ��������������������ϸ���͵��˾���ϸ����LPS�Ĵ̼��£�iNOS mRNA������ǿ��iNOS�������߲��ϳɴ�����NO��NO�������̼��շ�������ϸ���͵��˾���ϸ������ tNF���Ͱ��ص���֢������4�������ٽ�ǰ�����ص���֢���ʵĺϳ���5�������ǹ�ͬ�����γ��Ժ����֢�߷塣
��������Ĥ�ķ�����չ�Ƕ��������õĸ��Ӳ������̣����о���ʾ0 hʹ��L-NAME����������Ĥ�ף�����δ�ָ���������ˮƽ��˵��������������Ĥ�ײ������̵�ijЩ���棬���������л��ڡ�
���������
������1�ݡ�Moncada s, Higgs A. The L-arginine-nitric oxide pathway��J��. N Engl J Med,1993,329(27):2002-2012��
������2�ݡ�Tilton RG, Chang K, Corbett JA, et al. Endotoxin-induced uveitis in the rat is attenuated by inhibition of nitric oxide production��J��. Invest ophthalmol Vis Sci, 1994,35(8):3278-3288.
������3�ݡ�Kubes P, Granger DN. Nitric oxide modulates microvascular permeability��J��. am J Physiol, 1992,262(2 Pt2):H611-H615.
������4�ݡ�Liew FY. Interactions between cytokine and nitric oxide��J��. Adv neuroimmunol, 1995,5(2):201-209.
������5�ݡ�Salvemini D, Misko TP, Masferrer JL, et al. Nitric oxide activates cyclooxygenase enzymes��J��. Proc Natl Acad Sci USA, 1993,90(15):7240-7244.
������6�ݡ�Halliwell B. Oxygen radicals, nitric oxide and human inflammatory joint disease��J��. Ann Rheum Dis, 1995,54(3):505-510.
������7�ݡ�Furfine ES, Harmon MF, Paith JE, et al. Selective inhibition of constitutive nitric oxide synthase by NG-nitro-L-arginine��J��. biochemistry, 1993,32(33):8512-8517.
������8�ݡ�Mandai M, Yoshimura MN, Yoshida M, et al. The role of nitric oxide synthase in endotoxin-induced uveitis:effect of NG-nitro-L-arginine��J��. invest Ophthalmol Vis Sci, 1994,35(10):3673-3680. ��һҳ [1] [2] |
