|
����
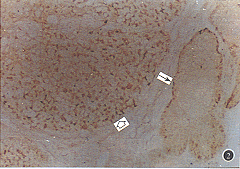 ͼ2��PCNA�������ٰ��еı���ڽ�����PCNA����ϸ���������ң��������ֲ�(�ռ�ͷʾ);���������Ե����ֳ��ʢ��ϸ���пɼ�ɢ�ڵ����Է�Ӧϸ��(ϸ��ͷʾ)����100 ͼ2��PCNA�������ٰ��еı���ڽ�����PCNA����ϸ���������ң��������ֲ�(�ռ�ͷʾ);���������Ե����ֳ��ʢ��ϸ���пɼ�ɢ�ڵ����Է�Ӧϸ��(ϸ��ͷʾ)����100
��������P53����PCNA���������������еı���
����102����������������֯�����зֻ��Ϻõİ���֯�У�P53�������Ա���ǿ����ҪΪ+;���ͷֻ���δ�ֻ��İ���֯�У�P53�������Ա���ǿ����ҪΪ++��+++����ͳ��ѧ��������SCC��P53�������Ա���ǿ������֯�ֻ��̶�֮�������������(P<0.05��Hc=7.12)�����������ֻ��̶ȵĽ��ͣ�3����������������PIֵ�����������ƣ�������������(��P<0.05����2)��
������2��P53����PCNA���������������еı���
�����걾����P53����P53����
����������(%)PIֵ
����(
 ��s��%)������� ��s��%)�������
����-++++++
����BCC53231111856.638.1��31.1
�����ֻ���261283353.928.6��26.0
����δ�ֻ���271138559.347.6��33.2t=2.348 8*
����SCC321695250.038.3��30.1
�����߷ֻ�14931135.727.4��25.1
�����зֻ�14752050.035.7��28.0
�����ͷֻ�40121100.083.9��12.1F=8.01*
���������ٰ�17715458.842.6��32.0
�����߷ֻ�5401020.018.9����9.7
�����зֻ�5112180.038.1��31.0
�����ͷֻ�7202385.762.7��32.7F=3.860 2*
����*P<0.05��������P53����������PCNAָ���Ĺ�ϵ
����102����������������֯������P53�������Ա������������������֯�У�PCNAƽ��ָ����������P53���Ա�����(P<0.05);����P53���Լ�������ߣ�PCNAָ�������ߵ����ƣ�����P53���ױ�����PCNA����������(��3)��
������3��P53����������PCNAָ���Ĺ�ϵ
�����걾P53����P53����tֵPֵ
��������PIֵ
����(
 ��s)����PIֵ ��s)����PIֵ
����(
 ��s) ��s)
����BCC3046.9��32.52328.3��26.02.2<0.05
����SCC1650.1��28.91626.5��26.52.2<0.05
���������ٰ�1056.6��33.0��722.5��17.22.6<0.05
�������ۡ���һ��P53����
������?[3]�����������������о�ǰ��λ�߷ֱ���BCC�������ٰ���SCC ������������ȷ�в���Ŀǰ�в���������������ٴ�ʵ���о�֤ʵ�������������������������Ϊ�Ŵ����������Ⱦɫ����쳣����һ�����о��������°�����������ϸ�����Ŵ�����(��Ҫ��DNA)�������Ŵ�����ĸı䣬 ʹijЩ�ؼ���ϸ�����ƻ���ͻ�����������P53 ����ͻ�䱻��Ϊ��Ŀǰ��֪��������������Ļ���ı�[1]���������ƻ���P53λ������17��Ⱦɫ��̱�(17P13.1)�ϣ�����������Է�������Ϊ53��103�ĺ������ף���Ϊ�������ͣ�Ұ����P53(WTP53)��ͻ����P53(MTP53)�������ļ�WTP53������ϸ�������������ã� �书����ͨ���յ�����ϸ����ֳ���õĻ���ת¼ʵ��[4]����л�����Ҫ��WAF1/CIP1��GADD45��IGF-BP3�� Bax ��mdm2�������DNA�������ˣ�P53�����ۣ�WAF1/CIP1 �Ȳ������ֻ�м��ͱ��DNA����ֹͣ��ʹ�����㹻��ʱ�������˵�DNA������ʧ�ܣ����յ�ϸ������,�Ӷ���ֹ�а�������ϸ���IJ���[5]�������P53������ͻ�䣬���������ƹ���ɥʧ������ϸ����ֳ�쳣��Ծ�����յ��������ķ���������ϸ���ڽ�������������P53���ף����ܿ콵�⣬���������黯�������Ѽ���ͻ����P53���������ı䣬�ȶ������ӡ���˥���ӳ�����Сʱ���ϣ���������������黯���������Ƿ���ͻ���P53���ף�P53����ͻ����P53���������ĸ߶�һ�����ѱ�֤ʵ[6]��PCNA�����ϸ�� DNA�ϳ��������һ����Է�������Ϊ36��103�ĺ˵��ף���DNA���ø�ĵĸ������ף���ϸ��DNA�ϳ��ڱز����ٵ�����[7]���ھ�ֹϸ����PCNA�������٣�G1���ڿ�ʼ���ӣ�S�ڴﵽ�߷壬G2�ڡ�M�������½�[8]�� �����ΪPCNA����Ϊ����ϸ����ֳ״̬����Ҫָ�ꡣ
��һҳ [1] [2] [3] ��һҳ |
