�� �ٴ�����
����һ��35������Ի���˫�������½�������Ϊ�Լ�����û�дﵽ���������������ڹ�ȥ�ļ���������һֱ���½���������ʹ�ģ������ڼ�ʻʱ�ѿ�����·�ꡣ
��������������֢��ʷ�����ð�����ͪ��һ��ǰ���ؼ���5���������Լ���Ϊ������֢��ԭ��ż���Ⱦƣ�������ҩ��ʷ��
������2��ǰ��һ��Ħ�г��¹���ʧȥ��ʶ��CT��ʾͷ��û���쳣��
������������20/60������20/80�� Ishiharaɫä�������ԡ�ͫ��Ծ���ȴ������ͫ�״����ϰ���˫����ѹ15 mmHg��˫��������Ұȱ��
������϶�Ƽ����ǰ���������۵����ɼ�˫�����̲ף���������֢��
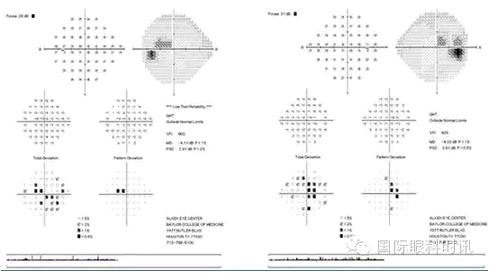
����ͼ1.�Զ���Ұ�����ʾ˫��������Ұȱ��
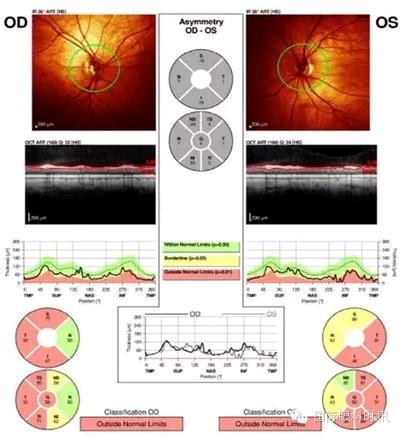
����ͼ2.��ѧ��ɶϲ�ɨ����ʾ˫�۵�����Ĥ����ά��ı䱡
�����������
�������ݻ��߶���Գ���˫�������½��IJ�ʷ�������Ϊ�Ŵ��������䡣����������Ŵ��������䣬�����Ŵ�������ή����������Ϊ���ڵ�֢״��������������Щ������Ӫ���Ժ��ж�����������ٴ��������ơ�
������֢��������������۾��˶�����ʹ���Ӽ��Ի��Ǽ��Է������Ӿ���ʧ����Щ֢״�������������йء�
����ȱѪ��������ᵼ�¼�������ɥʧ�������Ӿ������ȶ���
�������ڻ���˫�۳��������½��IJ�ʷ�����ų������������䡣����������½��Ļ�����ͷ�����沿ײ�������������Ӿ���ʧ�йء�
��������������ѹ����������������뱭�̱������йء��������û�г��ֱ��̱�������������Ұȱ�ݡ�������ۻ����Dz�����ֵġ�
�����ٴ����
�������ԴŹ��������ʾû���鲡�����ǿ�źţ�˫�۶ཹ����Ĥ��ͼ������
������Ϊ���ߵ����ؼ���ʷ�����ж��Ժ�Ӫ��������������ų�������ȫѪϸ��������Ҷ���ά����A��ά����B12����B1�ⶨ���ؽ����������ڵ����еIJ��Խ����������
�����Ի��ߵļ��岡ʷ�Ļع���ʾ�������游���������˵IJ�ʷ����û����ȷ�����Ϊ�����䣬Ҳû������ʷ��
�������黼�߸���ʱ���������游��������������ή�������⡣
��������
�����û������̲ײ��н����������½���������ļ���ʷ����Щ�о������ʾ���û����������Ŵ�������ή�����Ŵ���������ij�Ⱦɫ�������Ŵ�ģʽ��
�����ж��Ժ�Ӫ������������Ա���Ϊ���Ƶ�֢״������������ή�����ж��Ժ�Ӫ�����������У�����ͫ��Ӧ������������ͷ�ư��������ѡ���ԣ�����������ϸ����
����������쳣������� OPA1����λ��3��Ⱦɫ���ϡ�OPA1 �����䵰�ײ��GTP���ף������������л�����ٴ��Ƕ���������������߳�������ɥʧ���������ٵļ���������֢״��������������ʧ�������´����ۼ����(��������ή��)����������ή���Ļ�����ܲ�������ȫ���쳣֢״��
����OPA1 �����ͻ���в�ͬ�������ӱ�������Ϊ���Ӿ������ϰ�ˮƽ�������Ҫԭ��
��������ɥʧ�ķ�������ʼ��������ʱ�ڣ����ڹ�ȥ�ļ������������ä��������Ұȱ������ͷ�ư��������ܵ�Ӱ�죬��ʹ���̲ס�����������Ľ�չ����������Ĥ���׳��֡�
�������������Ŵ�������ή������������½���Ŀǰ��û����֮��Ч�����Ʒ����� ��Ȼ�����Ȼᱣ���ȶ�����һЩ�������Ų����չ�����������½���
���������
����1.Fraser JA, Biousse V, Newman NJ. The neuro-ophthalmology of mitochondrial disease. Surv Ophthalmol. 2010;55:299-334.
����2.Grzybowski A, Zulsdorff M, Wilhelm H, Tonagel F. Toxic optic neuropathies: an updated review. Acta Ophthalmol. 2015;93:402-410.
����3. Newman NJ. Treatment of hereditary optic neuropathies. Nat Rev Neurol. 2012;8:545-556.
����(��Դ���������ۿ�ʱѶ���༭��) |
